高一化学知识点总结
高一年级化学必背知识点包括以下几个方面:常温常压下为气态的有机物主要有:1~4个碳原子的烃,一氯甲烷、新戊烷、甲醛。碳原子较少的醛、醇、羧酸如甘油、乙醇、乙醛、乙酸易溶于水;而液态烃、卤代烃、硝基化合物、醚、酯等则难溶于水;苯酚在常温下微溶于水,但高于65℃时任意比互溶。
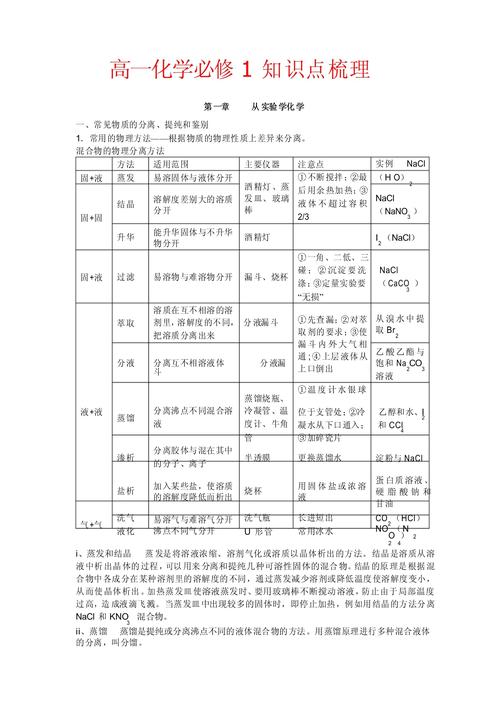
重点一:混合物分离与提纯常用物理方法 具体包括:实验室安全操作的“六防”,如预防爆炸、失火、中毒、倒吸、污染等;实验室意外事故的处理方法,如着火、割伤、烫伤、灼伤、腐蚀(浓酸、浓碱等)和中毒等。
非电解质、弱电解质、难溶于水的物质,气体在反应物、生成物中出现,均写成化学式或分式。固体间的反应,即使是电解质,也写成化学式或分子式。氧化物在反应物中、生成物中均写成化学式或分子式。
胶体 在1—100之间 均匀、有的透明、较稳定 能有 FeOH3胶体 浊液 大于100 不均匀、不透明、不稳定 不能 没有 泥水 物质的化学变化 物质之间可以发生各种各样的化学变化,依据一定的标准可以对化学变化进行分类。
【篇一】 基本概念 区分元素、同位素、原子、分子、离子、原子团、取代基的概念。正确书写常见元素的名称、符号、离子符号,包括IA、IVA、VA、VIA、VIIA族、稀有气体元素、1~20号元素及Zn、Fe、Cu、Hg、Ag、Pt、Au等。物理变化中分子不变,化学变化中原子不变,分子要改变。
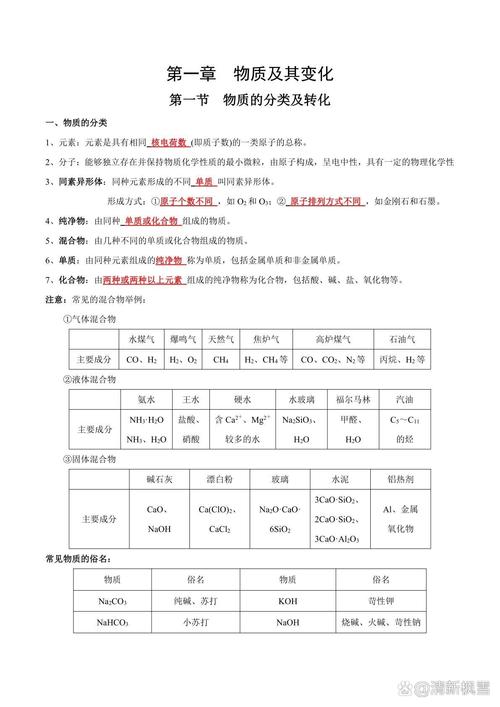
高一化学知识点有哪些?
高中化学第一册主要学习-氧化还原反应、碱金属、物质的量、物质的量的浓度、卤素、元素周期律、氧族元素、碳族元素。高中第二册主要学习-氮族元素、化学平衡、溶液的电离平衡、pH、几种重要的金属(铝、镁)、盐类的水解、有机物、糖、蛋白质。
高一年级化学必背知识点包括以下几个方面:常温常压下为气态的有机物主要有:1~4个碳原子的烃,一氯甲烷、新戊烷、甲醛。碳原子较少的醛、醇、羧酸如甘油、乙醇、乙醛、乙酸易溶于水;而液态烃、卤代烃、硝基化合物、醚、酯等则难溶于水;苯酚在常温下微溶于水,但高于65℃时任意比互溶。
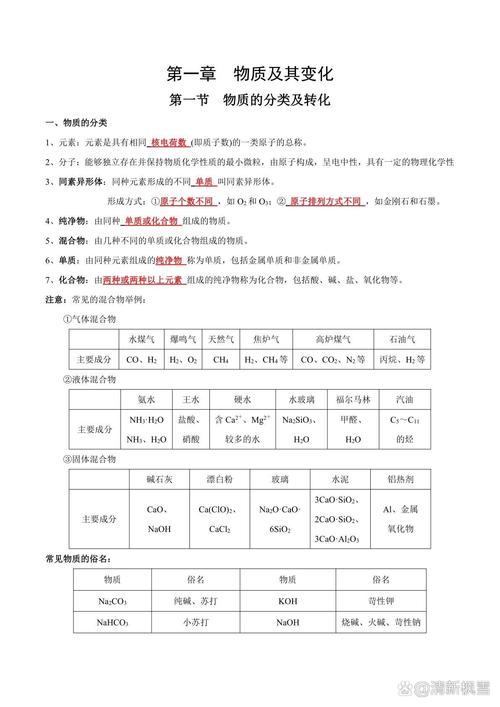
重点聚集 物质及其变化的分类 离子反应 氧化还原反应 分散系 胶体 知识网络 物质及其变化的分类 『1』物质的分类 分类是学习和研究物质及其变化的一种基本方法,它可以是有关物质及其变化的知识系统化,有助于我们了解物质及其变化的规律。
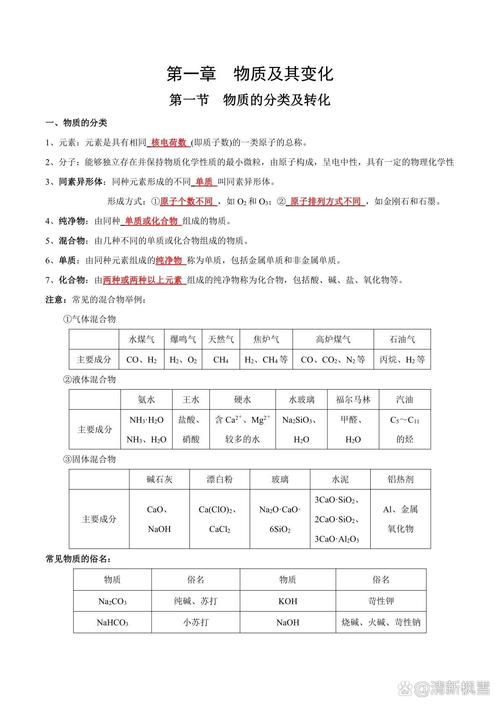
高一合格考化学必背知识点
首先,元素周期表是化学学习的基础,它不仅排列了元素,还揭示了元素之间的关系。周期表中元素的性质和特点通过周期性规律展现,学习时需注意周期表的排列原理。接着,化学键是化学反应的核心,包括原子间的化学键、离子间的化学键、共价键等。
山东省化学合格考涵盖了多个必考知识点,主要包括物质分类、元素与化合物、化学反应、摩尔与摩尔质量、气体状态方程、电化学、化学平衡、化学键、酸碱溶液以及有机化合物。物质分类是指根据物质的性质和组成将其分为纯物质和混合物,纯物质进一步分为元素和化合物,混合物则是两种或多种纯物质的混合。
如3AlO2-+3Al3++6H2O=4Al(OH)3↓等。化学合格考的知识点归纳 SO2的性质:强的还原性、漂白性、弱的氧化性、酸性氧化物。 SO2通入氯化钡、氯化钙溶液都没有沉淀。但是通入硝酸钡溶液有沉淀。
海南化学合格考必考知识点如下:气态物质在水中的溶解性 对气态物质来说,除了可以用溶解度来表示其溶解性以外,还可以用“吸收系数”来表示其溶解性(一定温度下单位体积的溶剂所能吸收的气体体积数)。
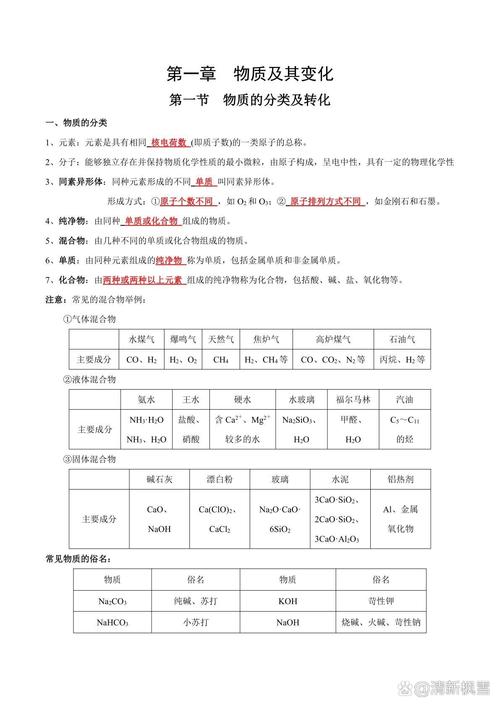
高一化学知识点是什么?
〖One〗、高一年级化学必背知识点包括以下几个方面:常温常压下为气态的有机物主要有:1~4个碳原子的烃,一氯甲烷、新戊烷、甲醛。碳原子较少的醛、醇、羧酸如甘油、乙醇、乙醛、乙酸易溶于水;而液态烃、卤代烃、硝基化合物、醚、酯等则难溶于水;苯酚在常温下微溶于水,但高于65℃时任意比互溶。
〖Two〗、高中化学第一册主要学习-氧化还原反应、碱金属、物质的量、物质的量的浓度、卤素、元素周期律、氧族元素、碳族元素。高中第二册主要学习-氮族元素、化学平衡、溶液的电离平衡、pH、几种重要的金属(铝、镁)、盐类的水解、有机物、糖、蛋白质。
〖Three〗、对于高一的学生而言,化学的必背知识点涵盖了化学元素周期表、电子结构、化学键和化学方程式等内容。这些知识点是化学学科中最基本、最重要的部分,掌握它们有助于学生更好地理解后续知识内容,并在考试中取得更好的成绩。高一化学的学习不仅仅局限于理论知识,还需要培养一定的化学实验能力。
〖Four〗、高一化学知识点有:产生有毒气体的实验应在通风橱中进行。常见的电解质指酸、碱、盐、水和金属氧化物,它们在溶于水或熔融时都能电离出自由移动的离子,从而可以导电。非电解质指电解质以外的化合物(如非金属氧化物,氮化物、有机物等);单质和溶液既不是电解质也不是非电解质。

高一化学基础知识点总结
高一年级化学必背知识点包括以下几个方面:常温常压下为气态的有机物主要有:1~4个碳原子的烃,一氯甲烷、新戊烷、甲醛。碳原子较少的醛、醇、羧酸如甘油、乙醇、乙醛、乙酸易溶于水;而液态烃、卤代烃、硝基化合物、醚、酯等则难溶于水;苯酚在常温下微溶于水,但高于65℃时任意比互溶。
氯及其化合物的性质 『1』氯气与氢氧化钠的反应:Cl2+2NaOH=NaCl+NaClO+H2O。『2』铁丝在氯气中燃烧:2Fe+3cl2点燃===2FeCl3。『3』制取漂白剂(氯气能通入石灰浆)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O。『4』氯气与水的反应:Cl2+H2O=HClO+HCl。
高一化学合格考中,需要掌握的知识点众多,这里列出几项重点内容。首先,元素周期表是化学学习的基础,它不仅排列了元素,还揭示了元素之间的关系。周期表中元素的性质和特点通过周期性规律展现,学习时需注意周期表的排列原理。
高中化学必修一知识点总结包括:研究物质性质的方法和程序,基本方法有观察法、实验法、分类法、比较法。基本程序:观察现象、分析、综合、推论,概括得出结论。钠及其化合物的性质,包括钠在空气中氧化、燃烧、与水反应等,伴随有熔化、浮于水面、生成银白色小球、响声及酚酞变红等现象。
高中化学第一册主要学习-氧化还原反应、碱金属、物质的量、物质的量的浓度、卤素、元素周期律、氧族元素、碳族元素。高中第二册主要学习-氮族元素、化学平衡、溶液的电离平衡、pH、几种重要的金属(铝、镁)、盐类的水解、有机物、糖、蛋白质。

高一化学学什么知识?
〖One〗、高中化学第一册主要学习-氧化还原反应、碱金属、物质的量、物质的量的浓度、卤素、元素周期律、氧族元素、碳族元素。高中第二册主要学习-氮族元素、化学平衡、溶液的电离平衡、pH、几种重要的金属(铝、镁)、盐类的水解、有机物、糖、蛋白质。
〖Two〗、高一化学主要学习的内容包括化学的基本概念、物质的分类、化学反应的基本规律、化学方程式、原子结构、元素周期表、化学键理论、溶液的性质、酸碱理论、氧化还原反应等。学生将学习化学是什么,它研究的对象和范围,以及化学在日常生活中的应用。
〖Three〗、此外,高一化学还涉及了化学键和化学反应的知识。学生学习了离子键、共价键和金属键等不同类型的化学键,以及化学反应的原理,包括化学方程式、化学平衡和反应速率。化学键的理解帮助学生更好地理解物质的结构和性质,而化学反应则揭示了物质间相互作用的本质。
〖Four〗、高一化学课程内容广泛,涵盖有机化学、无机化学、物质结构与性质、化学键以及化学反应等多个方面。学生通过实验和理论学习,不仅能掌握化学知识,还能提高实验技能,深入理解化学世界。有机化学部分,学生会学习有机物的结构、命名、性质和反应。
〖Five〗、下学期的课程继续深化对物质世界的认识,重点学习化学反应速率与平衡、电解质溶液、氧化还原反应等内容。学生们将学习如何计算化学反应中的物质的量,理解溶液的浓度与性质之间的关系,掌握电解质在水中的行为,探讨氧化还原反应的本质及其在日常生活中的应用。
〖Six〗、学生可以利用网络资源进行自主学习,也可以与同学交流学习心得,共同探讨问题。通过这样的方式,学生可以更深入地理解和应用所学知识。总之,高一化学课程的学习是一项系统工程,需要学生投入时间和精力,但通过努力学习,相信每位学生都能在化学的广阔天地中找到乐趣,并为今后的学习和生活打下坚实的基础。
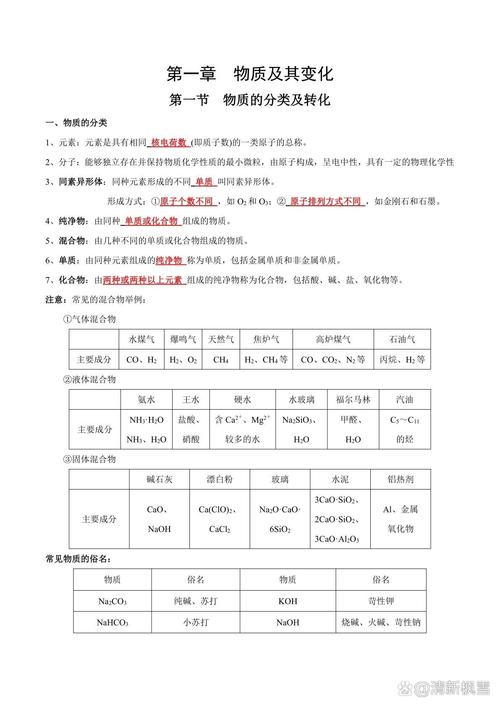
高一年级化学必背知识点
高一年级化学必背知识点包括以下几个方面:常温常压下为气态的有机物主要有:1~4个碳原子的烃,一氯甲烷、新戊烷、甲醛。碳原子较少的醛、醇、羧酸如甘油、乙醇、乙醛、乙酸易溶于水;而液态烃、卤代烃、硝基化合物、醚、酯等则难溶于水;苯酚在常温下微溶于水,但高于65℃时任意比互溶。
高中化学必背基础知识有:常见物质的颜色:有色气体单质:F2(浅黄绿色)、Cl2(黄绿色)、O3(淡蓝色)。
、能发生水解的物质:金属碳化物(cac2)、卤代烃(ch3ch2br)、醇钠(ch3ch2ona)、酚钠(c6h5ona)、羧酸盐(ch3coona)、酯类(ch3cooch2ch3)、二糖(c12h22o11)(蔗糖、麦芽糖、纤维二糖、乳糖)、多糖(淀粉、纤维素)(c6h10o5)n)、蛋白质(酶)、油脂(硬脂酸甘油酯、油酸甘油酯)等。
与化学高一相关的必修一知识点总结
〖One〗、与化学高一相关的必修一知识点总结1 化学反应的速率 『1』概念:化学反应速率通常用单位时间内反应物浓度的减少量或生成物浓度的增加量(均取正值)来表示。计算公式:v(B)== ①单位:mol/(L?s)或mol/(L?min)②B为溶液或气体,若B为固体或纯液体不计算速率。
〖Two〗、核素:具有一定数目的质子和一定数目的中子的一种原子。①质量数==质子数+中子数:A==Z+N ②同位素:质子数相同而中子数不同的同一元素的不同原子,互称同位素。
〖Three〗、化学方法分离和提纯物质 对物质的分离可一般先用化学方法对物质进行处理,然后再根据混合物的特点用恰当的分离方法(见化学基本操作)进行分离。用化学方法分离和提纯物质时要注意:①比较好不引入新的杂质;②不能损耗或减少被提纯物质的质量③实验操作要简便,不能繁杂。
〖Four〗、高一化学必背必考知识点必修一1 金属+酸→盐+H2↑中: ①等质量金属跟足量酸反应,放出氢气由多至少的顺序:AlMgFeZn。②等质量的不同酸跟足量的金属反应,酸的相对分子质量越小放出氢气越多。③等质量的同种酸跟足量的不同金属反应,放出的氢气一样多。 物质的检验 『1』酸(H+)检验。
〖Five〗、高一学年化学必修一重点知识点1 概念判断: 氧化还原反应的实质:有电子的转移(得失) 氧化还原反应的特征:有化合价的升降(判断是否氧化还原反应) 氧化剂具有氧化性(得电子的能力),在氧化还原反应中得电子,发生还原反应,被还原,生成还原产物。
〖Six〗、化学实验安全、过滤和蒸发 蒸馏和萃取 物质的量及其单位-摩尔 气体摩尔体积 物质的量在化学实验中的应用 物质的分类 离子反应、酸碱盐在水溶液中的电离、离子反应发生的条件 氧化还原反应:氧化剂和还原剂。金属及其化合物、金属与非金属、水的反应。
化学常识高一和高中化学知识点高一的介绍到此就结束了,如果能碰巧解决你现在面临的问题,别忘了关注本站,如果你还想了解更多这方面的信息,记得收藏关注本站,更多关于高中化学知识点高一的信息别忘了在本站进行查找喔。







还木有评论哦,快来抢沙发吧~